【背景】
与常见的碳酸酯溶剂相比,环醚溶剂,如1,3-二氧戊环(DOL),具有更低的冰点(-95℃)和粘度(0.6 cp),因此,在改善低温下的反应动力学方面具有很大潜力。然而,在低温电解质中使用DOL受到严重限制,因为它在无机盐(例如LiBF4、LiDFOB和LiPF6等)的存在下容易聚合,导致离子电导率严重降低,电化学行为恶化。DOL的聚合受阳离子开环机制的制约。具体来说,在有微量水存在的情况下,LiBF4等盐分解成BF3,很容易与H2O配位,形成质子酸H+(BF3OH)−。酸中的质子倾向于攻击DOL分子中氧的孤对电子,从而开始开环(图1a)。随后,DOL分子转变为碳原子,产生链式增长,然后导致聚合。为了防止这种聚合过程,以前的艺术主要致力于提高DOL分子的稳定性或在一定程度上锚定阴离子的积极反应。例如,在电解液中加入LiNO3能够通过DOL中NO3-和环氧键的配对位来抑制聚合过程,但不幸的是,由于NO3-和环氧键的强相互作用,这种策略牺牲了电极/电解液界面的离子流动性(电荷转移电阻的增加)。
回顾开环机制,作者注意到微量水通过为链的启动提供来源(质子)而发挥了关键作用,不幸的是,这在大多数情况下被忽视了。本工作目标是通过消除电解质中的微量水来防止DOL的开环聚合(图1b)。鉴于H2O是一种常见的亲核体,具有活性氢,作者提出了一种亲电子体,三甲基硅基异氰酸酯(Si-NCO),作为一种水清除剂,通过亲核加成反应消除H2O。因此,水被阻断提供质子,从而从根本上保护DOL免受开环聚合。由于吸电子共轭效应,Si-NCO的亲电中心是高度正电的,这大大促进了去除效率。此外,Si-NCO使DOL在很宽的温度范围内保持液体状态,即使是在高浓度的电解质中,这对低温操作至关重要。作者进一步证明,含有Si-NCO添加剂的新电解液与钴酸锂(LCO)阴极表现出良好的兼容性,在高容量、高速率能力和良好的循环稳定性方面实现了LCO||Li电池的体面低温性能。本工作的发现扩大了环醚溶剂在低温电解质中的应用,并突出了具有亲电性特征的水清除剂的设计的巨大空间。
【具体内容】
异氰酸酯的特点是带有-NCO基团,其中C=N键的C原子由于其低电子密度而作为亲电中心,很容易被H2O的O原子中的孤对电子所攻击,因此,有可能作为水清除剂。本研究特别选择了具有相同分子结构的异氰酸叔丁酯(C-NCO)和Si-NCO,因为它们的可用性和多功能性可以证明我们的设计(图1c)。将5vol%的C-NCO和Si-NCO加入到1M LiBF4/DOL电解液(表示为D1)中,分别形成D1/C-NCO和D1/Si-NCO电解液。如图2a所示,D1在环境中存放12小时后,由于DOL的聚合作用,彻底变成了凝胶状聚合物。然而,在电解质中加入Si-NCO和C-NCO似乎阻碍了DOL的聚合,显示出D1/Si-NCO保持其液体状态,而D1/C-NCO在储存12小时后仍处于半凝胶状态。显然,在防止聚合过程方面,Si-NCO比C-NCO更有效,尽管它们的分子结构相同。
为了研究水在启动DOL聚合中的作用,我们特意在LiBF4/DOL电解质溶液中加入500ppm的水(图2b)。氢核磁共振(NMR)光谱被收集在裸露的和添加了Si-NCO的样品上。位于4.65ppm和3.62ppm的化学位移可分别归属于聚合DOL(P-DOL)分子中A2和B2位点的1H原子;而位于3.34ppm的化学位移则对应于H2O分子中的1H原子。
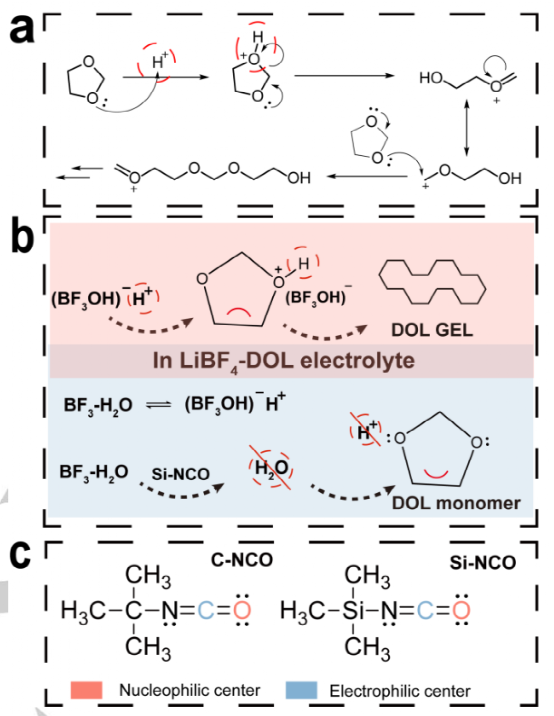
图1.(a) 显示DOL单体开环聚合过程的质子启动机制的示意图。(b) 防止DOL基电解质凝胶化的水清除剂的设计原理示意图。
图2c所示的1H NMR结果显示,在Si-NCO的存在下,指示H2O的峰消失了,表明Si-NCO很容易与H2O发生作用。我们还注意到,Si-NCO加入得越早,P-DOL的形成就越少,这明确地证明了这种相互作用有效地抑制了DOL的聚合。BF3来自LiBF4盐的分解,具有良好的配位H2O的能力,因此,在BF3存在的情况下,也研究了Si-NCO和C-NCO的水去除效率(图2d)。DME/BF3-2H2O混合物的红外光谱(IR)显示了3328和3670 cm-1之间的一个宽峰,它来自BF3-2H2O中的配位水(图2e)。与此形成鲜明对比的是,水的峰值强度在有C-NCO的情况下明显下降,而在有Si-NCO添加剂的情况下则完全消失,这表明即使溶剂中有BF3,Si-NCO仍能保持其高的除水效率。
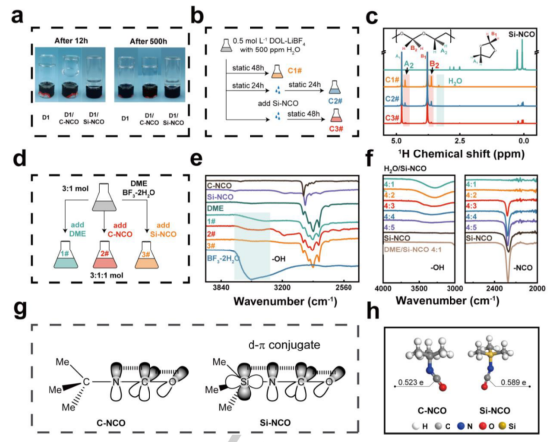
图2.异氰酸酯抑制DOL聚合的工作机制。
通过红外和密度泛函理论(DFT)计算,进一步描述了Si-NCO和H2O的反应机制。在H2O/Si-NCO混合物中,指示-OH振动的红外峰强度逐渐消失,而NCO(2278 cm-1)的强度随着Si-NCO浓度的增加而逐渐增强(图2f)。结合DME/Si-NCO(4:1)混合物中强烈的-NCO信号的结果,我们认为H2O/Si-NCO(4:1)中几乎检测不到的-NCO峰来自于与水的反应而不是浓度的限制,这意味着Si-NCO和水之间的相互作用主要是通过-NCO基团。这也与H2O和NCO之间的反应机制是由亲核加成反应支配的。为此,-NCO上的电荷分布基本上可以在决定反应速率方面发挥关键作用。尽管分子结构相同,但Si-NCO和C-NCO有两种类型的取代基,即C-NCO的叔丁基(-tBu)和Si-NCO的三甲基硅基(SiMe3)。据推测,Si-NCO化合物分子中Si的空三维轨道参与了d-π共轭的形成,而C-NCO对应物中则没有(图2g)。
此外,-SiMe3取代基是相对吸电子的,它在共轭体系中吸引电子,影响了基团内的电荷分布。因此,亲电中心,即Si-NCO的C=N键中的C原子,更具有电性,从而反过来加速了-NCO与水的反应速度。DFT计算表明,C-NCO和Si-NCO的C=N键上的C原子的电荷量分别为0.523 e和0.589 e(图2h)。电荷量意味着C原子位点的电子云密度的大小,较高的数值意味着较高的电子云密度,这与实验结果是一致的。鉴于Si-NCO和C-NCO在标准的1.0M LiBF4/DOL电解液中有效地抑制了DOL的聚合,研究它们在高浓度电解液中的可行性特别有意义,因为在这种溶液中聚合进行得更剧烈。
然后,我们在2.5M LiBF4的DOL/DME(体积比为7:3,记为DD2.5)中加入Si-NCO和C-NCO(2vol%),分别形成DD2.5/Si-NCO和DD2.5/C-NCO电解液。如图3a所示,DD2.5和DD2.5/C-NCO电解质在48小时后容易聚合,随后由于DOL的聚合,在储存2个月后变成石蜡状的白色固体,而DD2.5/Si-NCO在同一时间段内仍处于液体状态(图3a和图S3)。这种凝固过程增加了电解质的粘度,从而阻碍了Li+在溶剂中的流动性。因此,DD2.5电解质的离子电导率在储存48小时后从7.64 mS cm-1下降到0.45 mS cm-1,而添加Si-NCO的电解质则保持高度稳定(7.39至7.53 mS cm-1)(图3b)。这些结果清楚地表明,由于Si-NCO具有很高的除水效率,即使在高浓度LiBF4盐存在的情况下,它也能明显地防止DOL的聚合。图3c中的差示扫描量热法(DSC)曲线进一步证实,DD2.5/Si-NCO在广泛的温度范围内保持液态,直到温度下降到-105℃以下。
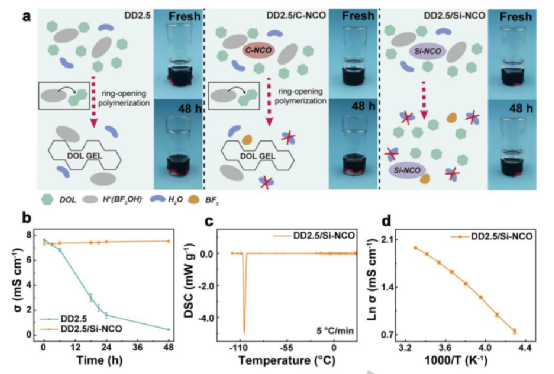
图3.低温下的电解质溶液的物理特性。
因此,DD2.5/Si-NCO电解质确保了Li+在低温下的快速传输,在温度下降到-40°C时表现出2.16 mS cm-1的高导电性(图3d)。DD2.5/Si-NCO在-40°C时仍保持液体状态。如此高的离子导电性完全满足了电池正常运行的要求,因此是低温下电化学性能大幅提高的原因。
如图4所示,DD2.5/Si-NCO电解质在LCO||Li电池中的实用性得到了进一步证明,并在低温下运行。在新鲜的DD2.5和DD2.5/Si-NCO电解质中,LCO阴极在25°C时的初始容量分别为128和140 mAh g-1(图4a)。然而,当电解质在环境条件下储存两个月后,使用DD2.5/Si-NCO电解质的电池仍然保持着126 mAh g-1的高容量(90%的容量保持率),而使用DD2.5电解质的电池由于电解质凝固导致离子传导性急剧下降而几乎降至零。随时间变化的电化学阻抗光谱(EIS)测量进一步证实了Li+在块体和界面的迁移率明显降低(图4b和4c)。用平衡电路拟合Nyquist图(图4b和4c的插图)导致欧姆(Rb)和电荷转移(Rct)电阻的分配,反映了离子迁移行为。在搁置17天后,使用DD2.5电解质的LCO||Li电池的Rb和Rct值分别增加了22.0和11.4倍。
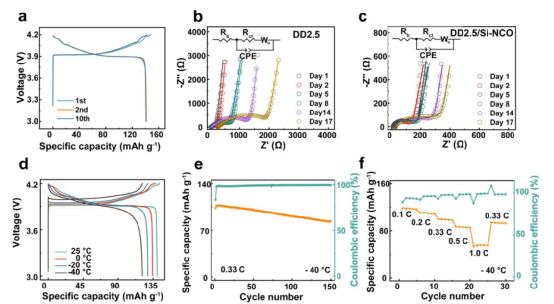
图4.LCO||Li电池的电化学性能。
与此形成鲜明对比的是,使用DD2.5/Si-NCO电解质的这些数值分别只增加了3.3和1.7倍,比DD2.5低一个数量级,这意味着Si-NCO有效地保持了高离子电导率,从而保持了快速电极反应动力学。这些特点保证了DD2.5/Si-NCO电解质在低温下工作时具有良好的电化学性能。因此,相对于25°C的温度,DD2.5/Si-NCO电解质中的LCO在0、-20和-40°C的容量保持率分别达到96%、91%和80%(图4d)。更引人注目的是,该电池表现出良好的速率能力(图4e)和出色的循环稳定性,在-40°C下循环150次后容量保持率为80%(图4f)。
DD2.5/Si-NCO电解液与LCO阴极完全兼容,因此,在低温金属锂电池的实际应用中具有很大的潜力。
除了界面动力学的增强,DD2.5/Si-NCO电解液显示出更高的抗氧化稳定性(图4a),这一点从LCO||Li电池的初始库仑效率(95%)比DD2.5电解液(80%)中的库仑效率的提高可以看出。我们假设在LCO表面构建了由Si-NCO添加剂诱导的稳定的阴极-电解质界面(CEI),该界面负责抑制阴极和电解质之间的后续副反应(如果有)。然后进行X射线光电子能谱(XPS)测量,研究LCO阴极上的界面化学性质(图5a-e),其中来自乙炔黑添加剂的C-C峰和LCO体贡献的M-O峰的信号较强,表明在DD2.5/Si-NCO电解液中形成的CEI较薄。这种CEI层的形成与LCO表面Si-NCO的先期分解密切相关,NxOy(图5d)和Si-O(图5e)物种的明显信号进一步证实了这一点。
RO-Li信号与电解质分解产物有关,如ROCO2Li和聚碳酸酯,而C-O、C=O和-CO3物种则来自醚类溶剂分子的氧化。对无机物(用F峰表示)和含氧有机物(用O峰表示,M-O除外)的相对含量进行定量分析,发现在DD2.5/Si-NCO衍生的CEI中,无机物的比例高于DD2.5电解液中的无机物(图5f)。显然,Si-NCO添加剂促进了LCO表面薄而无机物丰富的CEI的形成,因此,有利于在界面上建立稳定和快速的Li+传输。
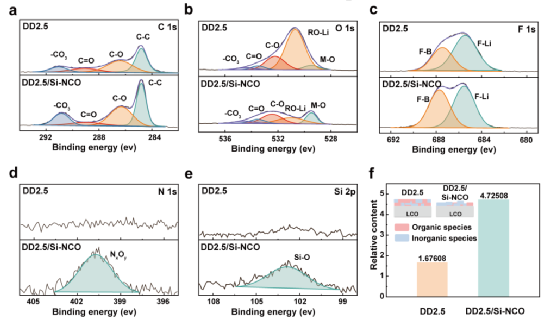
图5.LCO电极在DD2.5和DD2.5/Si-NCO电解质中的界面化学。
为了扩大设计概念的通用性,我们用其他无机盐,即LiPF6和LDFOB代替LiBF4进行验证。在LiPF6和LiDFOB盐的存在下,Si-NCO有效地抑制了DOL的聚合。尽管DOL与一些有机盐兼容,如LiTFSI,但基于LiFTSI的电解质中的电荷转移电阻和活化能(Ea)明显高于基于LiBF4的电解质,特别是在低温下。因此,使LiBF4与DOL溶剂兼容对于探索高性能的低温电解质是至关重要的。
【结论】
综上所述,提出了一种水清除剂Si-NCO来抑制DOL电解质的质子诱导的开环聚合,即使在高浓度LiBF4盐的存在下。
Si-NCO通过H2O和-NCO功能团之间的亲核加成反应来消除水分。由于d-π共轭,-SiMe3取代基是相对吸电子的,导致C=N键的C中心更具有电性,从而反过来加速了除水效率。因此,DD2.5/Si-NCO电解质具有相当低的冰点(-105°C)和低温下的高离子传导性(-40°C时为2.16 mS cm-1)。实际上,DD2.5/Si-NCO电解质与LCO阴极高度兼容,可提供80%的室温容量,并且在-40°C下循环150次后可保持80%的容量。对CEI界面的分析表明,Si-NCO的加入是导致CEI变薄和富含无机物的原因。我们的研究结果表明,水清除剂策略在环状醚基低温电解质的设计中具有高度的可行性。